1.完成半乳糖化海藻酸钠(G-SA)的合成与表征
1.1 半乳糖化海藻酸钠合成
称取0.15 g海藻酸钠溶于40 mL MES(0.2 M, pH 4.5)缓冲液中,搅拌3小时至完全溶解。加入17.5 mg NHS和363.05mg EDC(摩尔比EDC: COO-=2.5,NHS:EDC=0.2),室温搅拌30 min至均匀。加入245.1 mg半乳糖胺盐酸盐(摩尔比Gal:monosaccharide=1.5),室温反应24 h。反应产物置于截留分子量为10000的纤维素透析袋(广州菲薄生物科技有限公司)中,用去离子水透析3天,冻干。
1.2 半乳糖化海藻酸钠结构表征
FTIR 测试:取一定量的样品与溴化钾混合,研磨,采用溴化钾压片法,在 Nicolet/Nexus 670 FT-IR Analyzer(Nicolet Co., USA)上进行FTIR表征,扫描次数为 64 次,扫描范围为 400-4000 cm-1,分辨率为 4 cm-1。
1H NMR 测试:G-SA 溶于重水,利用 400 兆超导核磁共振谱仪 (Superconducting Fourier Transform Nuclear Magnetic, Bruker AVANCE 400)对样品结构进行 1H NMR 表征。
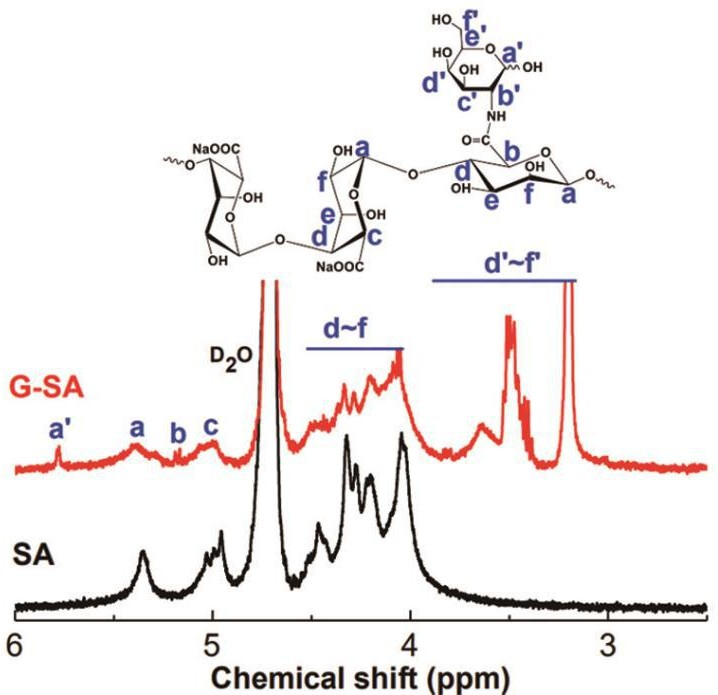
海藻酸钠和 G-SA 的氢谱
海藻酸钠和 G-SA 的红外谱图
2. 生物墨水制备
比例如下:table1 2
Table 1 Different composite of Bioink 1
|
Bioink
|
SA(g)
|
Gelatin(g)
|
H2O(mL)
|
|
A
|
0.4
|
0
|
10
|
|
B
|
0.4
|
0.6
|
10
|
|
C
|
0.4
|
0.8
|
10
|
|
D
|
0.4
|
1.0
|
10
|
|
E
|
0.4
|
1.2
|
10
|
Table 2 Different composite of Bioink 2
|
Bioink
|
G-SA(g)
|
Gelatin(g)
|
H2O(mL)
|
|
A
|
0.4
|
0
|
10
|
|
B
|
0.4
|
0.6
|
10
|
|
C
|
0.4
|
0.8
|
10
|
|
D
|
0.4
|
1.0
|
10
|
|
E
|
0.4
|
1.2
|
10
|
3. 支架打印
|
|
气压(Mpa)
|
填充间距(mm)
|
针头(G)
|
层数
|
|
Bioink 1-C
|
0.5
|
1.5
|
22
|
6
|
|
Bioink 2-C
|
0.5
|
1.5
|
22
|
6
|
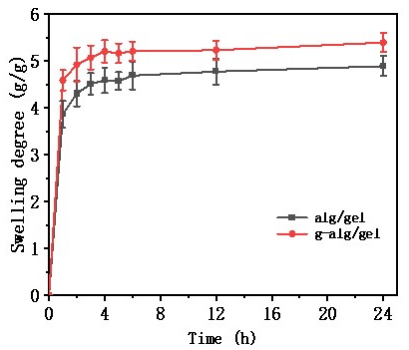
4. 打印支架溶胀率表征
实验步骤:打印好的支架经冷冻干燥 24 h 后取出,天平称取质量记录 Wd,置于 5 ml PBS 中,记录 1, 2, 3, 4, 5, 6, 12, 24 h的 质量记录 Ws。
5. 肝细胞培养实验
5.1 构建含绿色荧光蛋白的肝细胞(LO2)稳转细胞系
培养LO2细胞,待细胞长至80%~90%消化细胞并计数,按5*105cells/孔的细胞密度接种细胞到6孔板中;第二天换带有8 ug/ mL polybrene的完全培养基并以MOI=50(根据不同细胞而定)加入慢病毒;第三天换成完全培养基培养,48 h 后消化细胞并以1:2传代,细胞贴壁后按2ug/ mL(不同细胞浓度略有差异)的浓度加入 puromycin 做筛选,每2~3天换液(带2ug/ mL 的 puromycin 完全培养基);等细胞长满后消化细胞扩大培养,即可获得带绿色荧光蛋白的 LO2 稳转细胞。
5.2.荧光显微镜观察微凝胶与 LO2 稳转细胞系共培
培养含绿色荧光蛋白的稳转 LO2 细胞系,待细胞长至80%~90%消化细胞并计数,按5*105cells/孔的细胞密度接种细胞到 6 孔板中;取相同量的Gel-1海藻酸钠和Gel-3半乳糖化海藻酸钠微凝胶,分别加入对应的 6 孔板培养;分别于24小时和48小时后于倒置镜荧光显微镜(OLYMPUS IX71)观察两组的细胞
总结:已找到最合适的墨水配比,优化了打印条件,细胞增殖实验证明半乳糖化海藻酸钠水凝胶支架的优良性能,后续细胞实验将有序开展。
|